Укажите символ химического элемента:
Централизованное тестирование по химии, 2015
Число нейтронов в составе атома ![]() равно:
равно:
Элемент, атом которого в основном состоянии имеет электронную конфигурацию 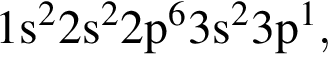 находится в группе:
находится в группе:
Согласно положению в периодической системе наименьший радиус имеют атомы химического элемента:
Ионная связь имеется во всех веществах ряда:
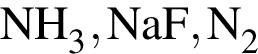
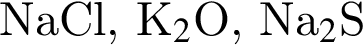
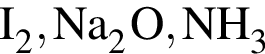
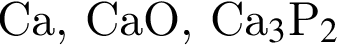
Атомную кристаллическую решетку в твердом агрегатном состоянии образует:
В атоме химического элемента ![]() в основном состоянии электроны распределены по энергетическим уровням следующим образом: 2, 8, 7. Степень окисления
в основном состоянии электроны распределены по энергетическим уровням следующим образом: 2, 8, 7. Степень окисления ![]() в высшем оксиде равна:
в высшем оксиде равна:
С помощью прибора, указанного на рисунке, способом вытеснения воды можно с минимальными потерями собрать газ:
Массовая доля кислорода в карбонате аммония:
Укажите НЕВЕРНОЕ утверждение:
Укажите НЕВЕРНОЕ утверждение:
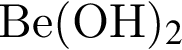 — это щелочь
— это щелочьОснования образуются в результате превращений:
а — 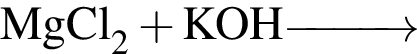
б — 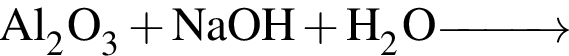
в — 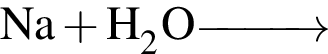
г — 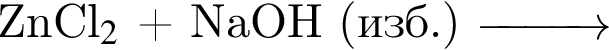
Используя в качестве реагента только разбавленную серную кислоту, в одну стадию НЕВОЗМОЖНО осуществить превращение:


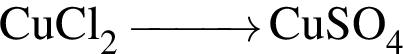
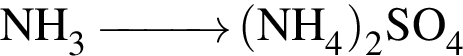
Относительно вещества, формула которого 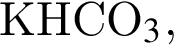 верно:
верно:
а — в водном растворе реагирует с углекислым газом
б — взаимодействует с раствором уксусной кислоты
в — относится к средним солям
г — при его разложении образуется карбонат калия
Выберите ряд реагентов, которые в указанном порядке можно использовать при осуществлении превращений по схеме ![]() →
→ 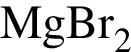 →
→ 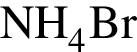 →
→ ![]() (электролиты взяты в виде водных растворов):
(электролиты взяты в виде водных растворов):
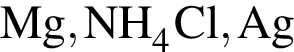
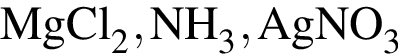
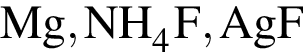
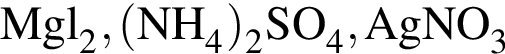
Оксид фосфора(V) проявляет кислотные свойства, реагируя с веществами:
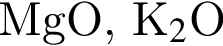
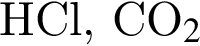
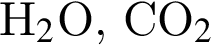
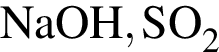
Понизить жесткость воды (20 °C) можно, добавив в нее:
a — ![]()
б — 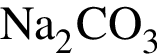
в — ![]()
г — 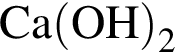
Цинковую пластинку погрузили в разбавленный водный раствор, в результате чего масса пластинки увеличилась. В исходном растворе находилось вещество:
Укажите НЕВЕРНОЕ утверждение:
В схеме превращений
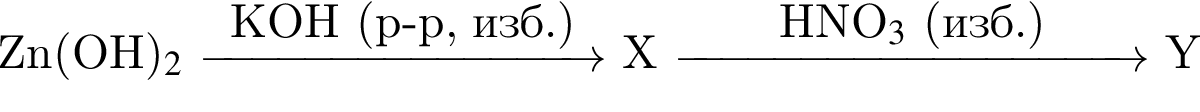
веществами ![]() и
и ![]() соответственно являются:
соответственно являются:
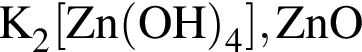
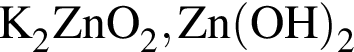
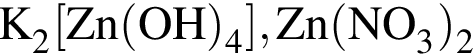
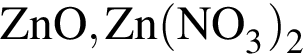
В результате гидратации оксида серы(VI) в соответствии с термохимическим уравнением
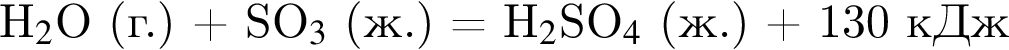
получена серная кислота массой 68,6 г. Количество теплоты (кДж), которая выделилась при этом, равно:
В закрытом сосуде протекает химическая реакция А + 2В = 2С + D. До начала реакции молярная концентрация вещества В равнялась 1 моль/дм3, а вещества D — 0 моль/дм3. Через сколько секунд концентрации веществ В и D сравняются, если скорость образования вещества D составляет 0,01 моль/дм3 · с (все вещества — газы, объем сосуда постоянный)?
При понижении давления в 4 раза при постоянной температуре в равновесной системе
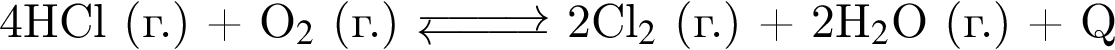 :
:
Имеется насыщенный водный раствор фторида бария. Осадок образуется при:
а — добавлении в раствор твердого фторида калия
б — упаривании раствора и последующем охлаждении до первоначальной температуры
в — добавлении в раствор твердого хлорида бария
г — добавлении в раствор дистиллированной воды
К раствору, содержащему смесь сульфида натрия и хлорида калия, прибавили избыток хлороводородной кислоты. К полученному раствору добавили избыток раствора нитрата серебра(I). Какие ионы присутствуют в конечном растворе (растворимостью в воде образующихся газов и осадков пренебречь)?
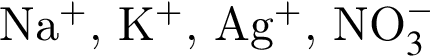
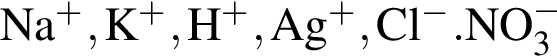
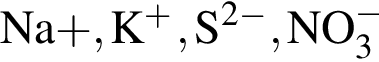
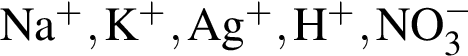
Выберите схему практически осуществимой реакции (указаны все исходные вещества и продукты реакций без коэффициентов):


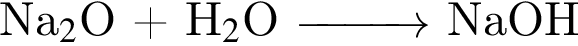

Соединение, формула которого относится к классу:
Продуктом реакции присоединения является 1,2-дибром-2-метилпентан.
Исходное вещество имеет название:
Выберите вещества, которые в указанных условиях реагируют с бензолом:
а — 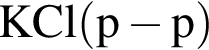
б — 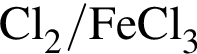
в — 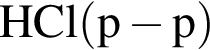
г — 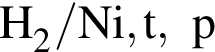
Продуктом превращения
является соединение:
Число структурных изомеров среди спиртов состава 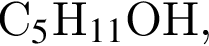 которые можно окислить до соответствующих карбоновых кислот состава
которые можно окислить до соответствующих карбоновых кислот состава 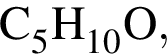 равно:
равно:
Фенол в отличие от этанола:
В результате окисления альдегида с помощью 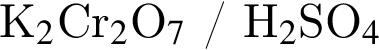 получена соответствующая кислота. При взаимодействии кислоты с этаналом в условиях кислотного катализа образовался сложный эфир состава
получена соответствующая кислота. При взаимодействии кислоты с этаналом в условиях кислотного катализа образовался сложный эфир состава 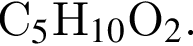 Укажите название альдегида:
Укажите название альдегида:
При полном щелочном гидролизе триглицерида получен стеарат натрия. Укажите формулу триглицерида:
Укажите верное утверждение относительно крахмала:
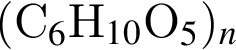
Амин, структурная формула которого представлена на рисунке:
а — является вторичным
б — является первичным
в — НЕ изменяет окраску раствора фенолфталеина
г — имеет название этанамин
Для соединения, формула которого представлена на рисунке, верно:
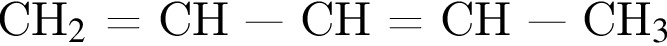
Число пептидных связей в молекуле
равно:
При действии воды на твердое вещество А образуется углеводород Б (легче воздуха). При присоединении к Б водорода получается углеводород В (также легче воздуха). В реакции В с водой в присутствии кислоты образуется соединение Г. При взаимодействии Г с муравьиной кислотой (в присутствии серной кислоты) получаются легкокипящая жидкость Д и неорганическое вещество Е. Найдите сумму молярных масс (г/моль) органических веществ Б, Г и Д.
Установите соответствие между органическим веществом и его изомером.
А) 2-метилпропанол-2
Б) гексен-1
В) пропадиен
Г) метилпропионат
1) бутановая кислота
2) бутанол-1
3) пропин
4) бутаналь
5) гексен-2
Ответ запишите в виде сочетания букв и цифр, соблюдая алфавитную последовательность букв левого столбца, например: А2Б1B3Г4.
Алкин массой 104,00 г полностью сожгли в избытке кислорода. Образовавшийся углекислый газ смешали с гелием объемом (н. у.) 56,00 дм3. Молярная масса полученной при этом смеси газов составила 34,20 г/моль. Определите молярную массу (г/моль) алкина.
Определите молярную массу (г/моль) соли, полученной в результате следующих превращений органических веществ:
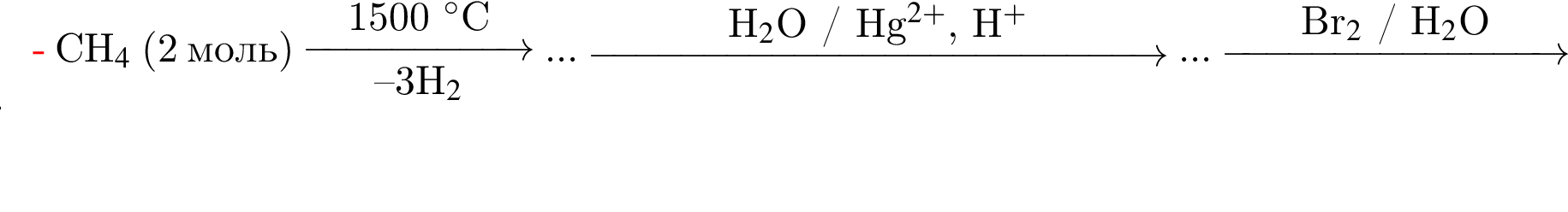
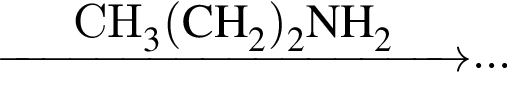
Выберите утверждения, характеризующие водород:
1) атомы в молекуле связаны ковалентной связью
2) плотность D2 равна 0,089 г/дм3 (н. у.)
3) с кислородом (при поджигании) в качестве основного продукта образует ![]()
4) при нагревании восстанавливает медь из оксида меди(II)
5) в лаборатории получают действием соляной кислоты на цинк
6) гидрид-ионы содержатся в водном растворе уксусной кислоты
Ответ запишите в виде последовательности цифр в порядке возрастания, например: 245.
Для получения веществ по указанной схеме превращений
![]() →
→ ![]() →
→ 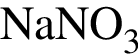 →
→ ![]() →
→ ![]()
выберите реагенты из предложенных:
1 — 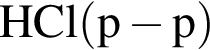
2 — ![]()
3 — 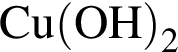
4 — 
5 — 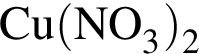
6 — ![]()
Ответ запишите цифрами в порядке осуществления превращений, например: 2443. Помните, что один реагент может использоваться несколько раз, а другой — не использоваться вообще.
В четырех пронумерованных пробирках находятся растворы неорганических веществ. О них известно следующее:
— вещества из пробирок 2 и 3 нейтрализуют друг друга, способны растворять цинк, его оксид и гидроксид;
— вещества из пробирок 3 и 4 реагируют между собой с образованием осадка, способного растворяться как в кислотах, так и в щелочах;
— при электролизе расплава вещества из пробирки 1 выделяется газ (н. у.) зеленовато-желтого цвета, имеющий характерный запах.
Установите соответствие между содержимым пробирки и ее номером.
А) гидроксид калия
Б) сульфат алюминия
В) азотная кислота
Г) хлорид натрия
1
2
3
4
Ответ запишите в виде сочетания букв и цифр, соблюдая алфавитную последовательность букв левого столбца, например: А2Б1В3Г4.
При прокаливании очищенного мела массой 320 кг получили 155,9 кг негашеной извести. Определите выход (%) продукта реакции.
Для анализа смеси, состоящей из ![]() и
и ![]() провели следующие операции. Навеску смеси массой 2,00 г растворили в воде. К полученному раствору прибавили 34,0 г раствора нитрата серебра(I) с массовой долей
провели следующие операции. Навеску смеси массой 2,00 г растворили в воде. К полученному раствору прибавили 34,0 г раствора нитрата серебра(I) с массовой долей 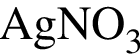 20%. Выпавший осадок отфильтровали , промыли, высушили и взвесили. Его масса оказалась равной 3,70 г. Вычислите массовую долю (%) ионов натрия в исходной смеси.
20%. Выпавший осадок отфильтровали , промыли, высушили и взвесили. Его масса оказалась равной 3,70 г. Вычислите массовую долю (%) ионов натрия в исходной смеси.
В результате полного восстановления оксида железа(III) углеродом была получена смесь угарного и углекислого газов количеством 1,1 моль и массой 43,6 г. Рассчитайте массу (г) образовавшегося при этом железа.
Для полного гидрирования газообразной смеси ациклических углеводородов (относительная плотность по гелию 13,5) необходим водород, объем которого вдвое больше объема смеси. Рассчитайте , какой объем (дм3) кислорода требуется для полного сгорания исходной смеси углеводородов массой 54 г (все объемы измерены при нормальных условиях).
Определите сумму молярных масс (г/моль) серосодержащих веществ Б, Е и алюминий содержащего вещества Д, полученных в результате превращений (Б является кислой солью)

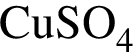 .
.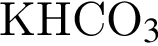 не взаимодействует с углекислым газом, являясь кислой солью.
не взаимодействует с углекислым газом, являясь кислой солью.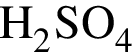 ) = 68.6/98 = 0.7 моль.
) = 68.6/98 = 0.7 моль.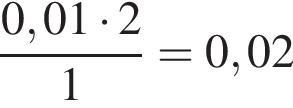 моль/дм3. Текущая концентрация вещества В рассчитывается по формуле C(В) = C0(B) − vB · t, а текущая концентрация вещества D по формуле C(D) = vD · t (v - скорости расходования и образования, соответственно). Найдем время:
моль/дм3. Текущая концентрация вещества В рассчитывается по формуле C(В) = C0(B) − vB · t, а текущая концентрация вещества D по формуле C(D) = vD · t (v - скорости расходования и образования, соответственно). Найдем время: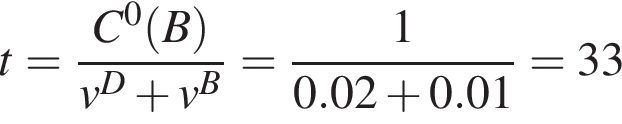 c
c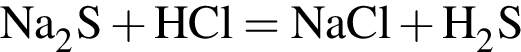 ↑
↑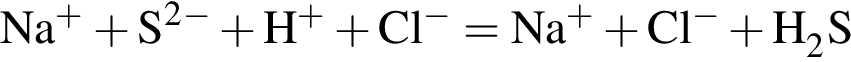 ↑
↑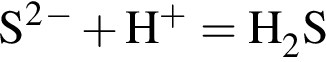 ↑
↑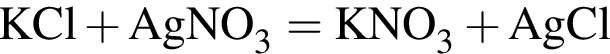 ↓
↓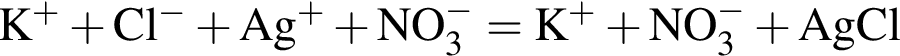 ↓
↓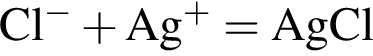 ↓
↓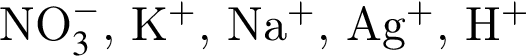 . Присутствие ионов серебра и водорода обуславливается добавлением избытков раствора нитрата серебра(I) и соляной кислоты к смеси.
. Присутствие ионов серебра и водорода обуславливается добавлением избытков раствора нитрата серебра(I) и соляной кислоты к смеси. , содержащие тройную связь между атомами углерода.
, содержащие тройную связь между атомами углерода.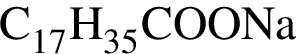 , значит, триглицерид имеет только кислотные остатки с химической формулой
, значит, триглицерид имеет только кислотные остатки с химической формулой 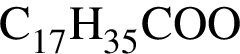
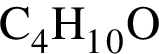 . Такую же формулу имеет бутанол-1.
. Такую же формулу имеет бутанол-1. 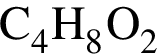 . Такую же формулу имеет бутановая кислота.
. Такую же формулу имеет бутановая кислота.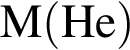 + n(
+ n(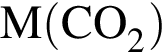 )/(n(
)/(n(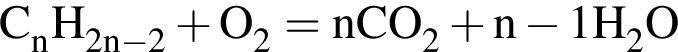
 = 7,7/n;
= 7,7/n;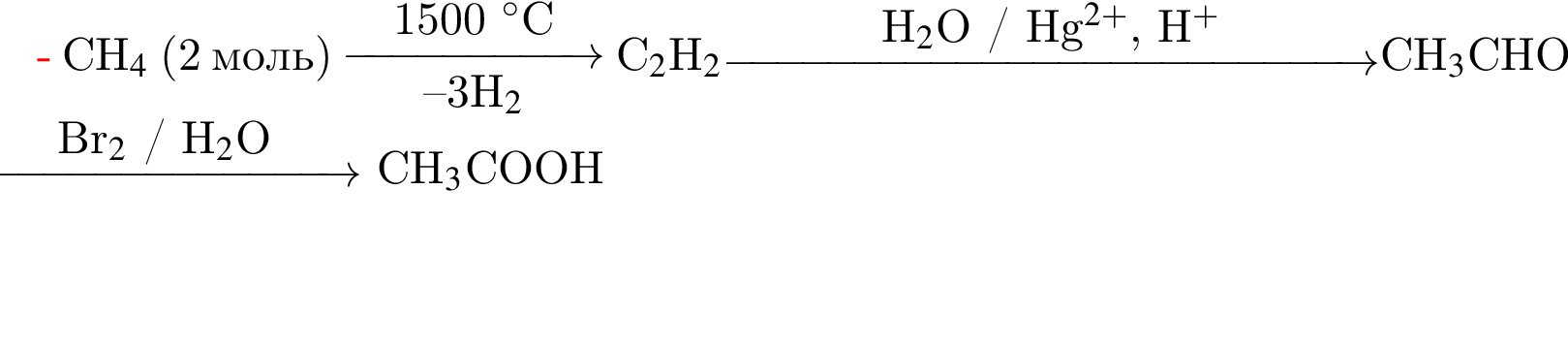
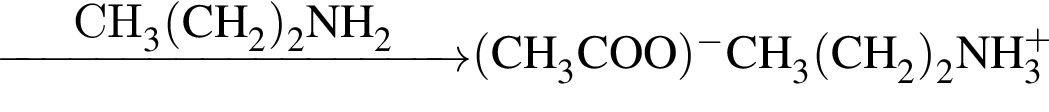
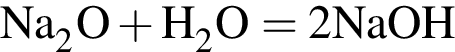
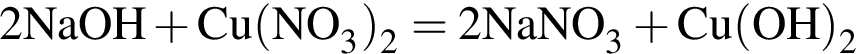
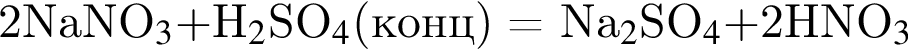
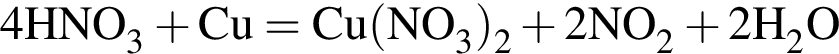
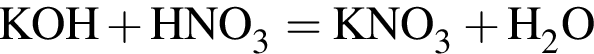
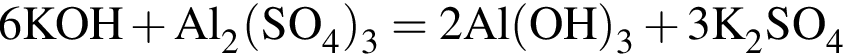
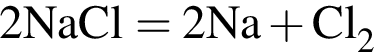 (зеленовато-жёлтый газ)
(зеленовато-жёлтый газ)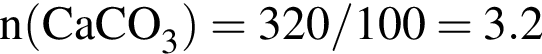 моль
моль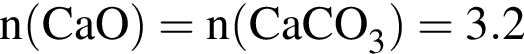 моль
моль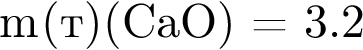 ·
· 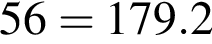 кг
кг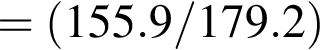 · 100%
· 100% 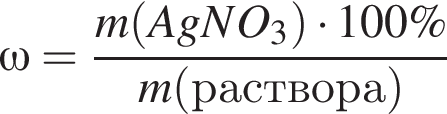
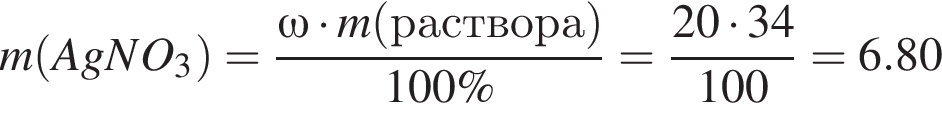
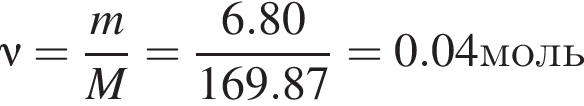
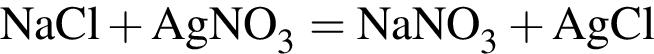 ↓
↓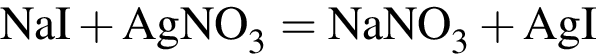 ↓
↓
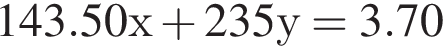
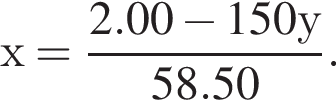 Подставим это выражение во второе уравнение системы.
Подставим это выражение во второе уравнение системы.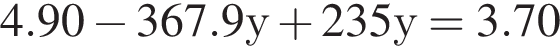 →
→ 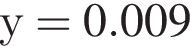 моль (
моль (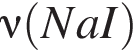 )
)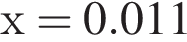 моль (
моль (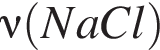 )
)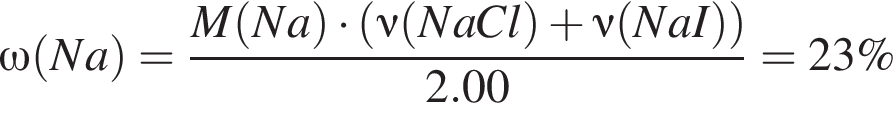
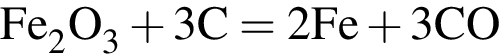
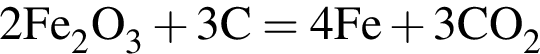
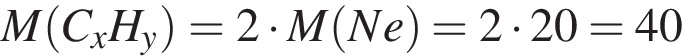 г/моль
г/моль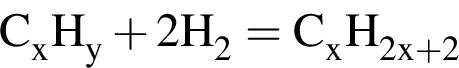
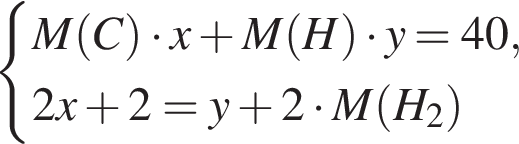
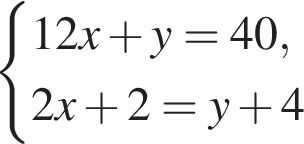
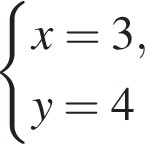
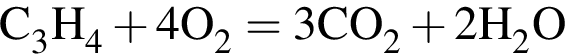
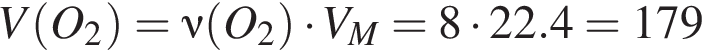 л
л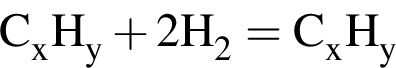
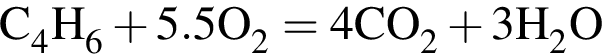
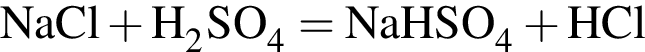 (А)
(А)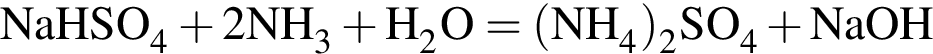 (Г)
(Г)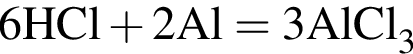 (В)
(В)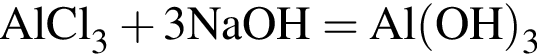 (Д)
(Д)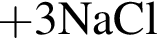
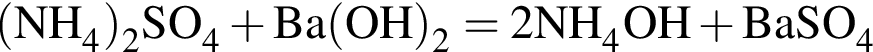 (Е)
(Е)